Para una correcta visualización, debes tener el dispositivo en posición horizontal.


En busca
del camino más directo
en Cáncer
Gastroesofágico

Este material es solo para su uso personal. No está permitida su reproducción o distribución.
Si desea obtener más información, consulte la Ficha Técnica autorizada de Opdivo que se facilita https://ira.redbms.es/IO-FTOpdivo
1506-ES-2400270 02/25 Fecha creación Febrero 2025



En busca
del camino más directo
en Cáncer
Gastroesofágico

Este material es solo para su uso personal. No está permitida su reproducción o distribución.
Si desea obtener más información, consulte la Ficha Técnica autorizada de Opdivo que se facilita https://ira.redbms.es/IO-FTOpdivo
1506-ES-2400270 02/25 Fecha creación Febrero 2025



CASO 1
ADYUVANCIA


Caso 1

Cáncer de esófago
Características demográficas y antecedentes personales
- Varón
- 50 años
- Fumador crónico
- Ex-enolismo desde hace un año
Enfermedad actual
- Paciente que acude a consultas externas por presentar disfagia progresiva a sólidos y a líquidos, acompañada de pérdida de peso de aproximadamente 5 kg en el último mes
Diagnóstico
- EDA: lesión ulcerada en esófago medio
- Biopsia: carcinoma epidermoide de esófago
- TC: tumor en esófago medio, a nivel de carina traqueal, con adenopatías locorregionales afectas. No enfermedad a distancia
- Estadificación preoperatoria: T3N1M0
- PET: captación de contraste en esófago inferior y adenopatías regionales
EDA: endoscopia digestiva alta; TC: tomografía computerizada; PET: tomografía por emisión de positrones.
*Las imágenes no corresponden a pacientes reales


Pregunta 1/5
Caso 1
¿Qué tratamiento perioperatorio consideras que sería recomendable realizar a este paciente?1,2
A) QRT definitiva
B) QRT neoadyuvante, según esquema CROSS
C) Esquema FLOT
D) Epirrubicina, cisplatino y 5-FU o capecitabina (ECF/ECX)
QRT: quimiorradioterapia; ECF: epirrubicina, cisplatino y 5-fluorouracilo; ECX: epirrubicina, cisplatino y capecitabina.
Esquema CROSS: neoadyuvancia con quimioterapia y radioterapia hiperfraccionada: Carboplatino: AUC 2 i.v. semanal (Días 1-8-15-22-29) Paclitaxel: 50 mg/m2 i.v. semanal (Días 1-8-15-22-29) Radioterapia: 41.4 Gy en 23 fracciones de 1.8 Gy cada una 5 días por semana. 1
Esquema FLOT4: 4 ciclos de quimioterapia basada en la combinación de fluorouracilo, leucovorina, oxaliplatino y docetaxel, administrado cada dos semanas. Afdministración durante cuatro ciclos preoperatorios, seguidos de cuatro ciclos postoperatorios. Cada ciclo de 2 semanas de FLOT consistió en docetaxel 50 mg/m2 el día 1, oxaliplatino 85 mg/m2 el día 1, leucovorina 200 mg/m² el día 1 y 5-FU 2600 mg/m² como infusión de 24 horas el día 1. 2
1. van Hagen P, Hulshof MC, van Lanschot JJ, et al. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med 2012; 366: 2074-84; 2. Al-Batran SE, et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomised, phase 2/3 trial. Lancet. 2019 May 11;393(10184):1948-1957.
Lorem ipsum dolor sit amet consectetur adipisicing elit. Itaque aut maxime, corrupti recusandae error debitis eos ratione. Excepturi aspernatur perferendis eos autem, alias ab porro, a perspiciatis, necessitatibus corrupti cum.
* Lorem ipsum dolor sit amet consectetur, adipisicing elit.


Pregunta 2/5
Caso 1
¿Qué criterio tendría que cumplirse para que este paciente sea subsidiario de tratamiento con OPDIVO® en adyuvancia?1
A) Enfermedad patológica residual
B) Resección quirúrgica entre 4 y 16 semanas antes del inicio del tratamiento
C) Estadio I/II de CE/CUGE
D) A y B son correctas
CE: cáncer de esófago: CUGE: cáncer de la unión gastroesofágico.
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203.
Lorem ipsum dolor sit amet consectetur adipisicing elit. Itaque aut maxime, corrupti recusandae error debitis eos ratione. Excepturi aspernatur perferendis eos autem, alias ab porro, a perspiciatis, necessitatibus corrupti cum.
* Lorem ipsum dolor sit amet consectetur, adipisicing elit.


Pregunta 3/5
Caso 1
En el estudio CheckMate 577, que evaluó el tratamiento con OPDIVO® en pacientes con CE / CUGE en adyuvancia, ¿cuál fue el objetivo principal del estudio?1
A) Supervivencia libre de progresión
B) Supervivencia global
C) Supervivencia libre de enfermedad
D) Supervivencia libre de evento
CE: cáncer de esófago: CUGE: cáncer de la unión gastroesofágica.
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203.
Lorem ipsum dolor sit amet consectetur adipisicing elit. Itaque aut maxime, corrupti recusandae error debitis eos ratione. Excepturi aspernatur perferendis eos autem, alias ab porro, a perspiciatis, necessitatibus corrupti cum.
* Lorem ipsum dolor sit amet consectetur, adipisicing elit.


Pregunta 4/5
Caso 1
¿Con qué frecuencia cabría esperar la aparición de efectos adversos inmunorrelacionados relevantes (grados 3 o 4) con el tratamiento con OPDIVO® en adyuvancia?1,2
A) 10-15%
B) 5-10%
C) 1-5%
D) ≤1%
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203; 2. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203. Material suplementario
Los AART seleccionados de posible etiología inmunológica de grados 3 y 4 en cualquier clase de órgano se presentaron en el 1% o menos de los pacientes del grupo de OPDIVO®, y no hubo eventos de grado 5 en esta categoría.1
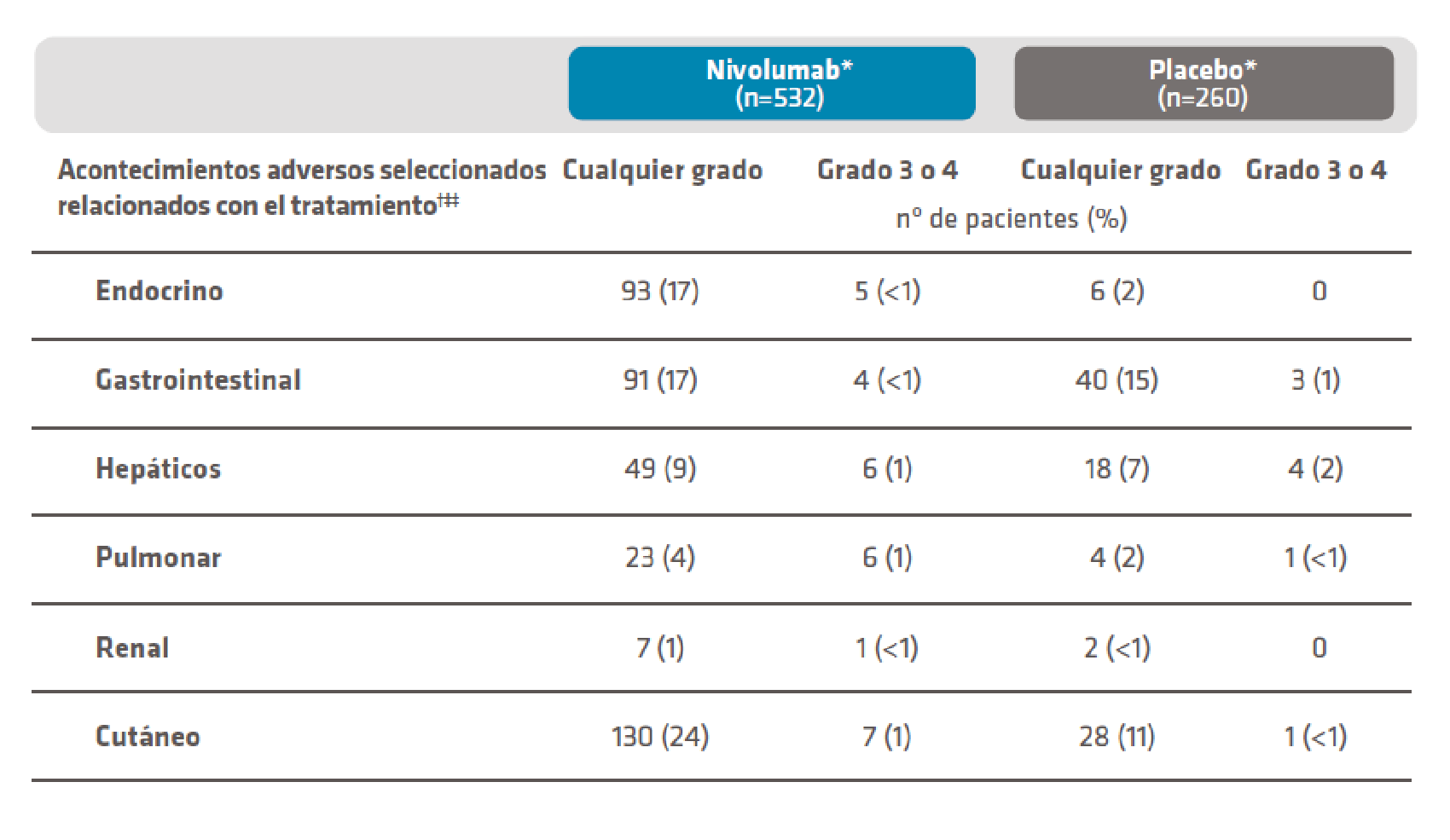
AART: Acontecimientos adversos relacionados con el tratamiento.
*Todos los pacientes aleatorizados que recibieron al menos una dosis del tratamiento del ensayo (población de seguridad).
†Los acontecimientos adversos seleccionados relacionados con el tratamiento son aquellos con potencial etiología inmunológica que requieren supervisión/intervención frecuente.
‡Acontecimientos notificados entre la primera dosis y 30 días después de la última dosis del fármaco del ensayo.
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203; 2. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203. Material suplementario


Pregunta 5/5
Caso 1
Indica en cuáles de los siguientes subgrupos existe una limitación del beneficio de la SLE en el estudio CheckMate 5771
Limitación
Sin limitación
SLE: supervivencia libre de enfermedad.
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203.
Los beneficios en SLE con OPDIVO® para el tratamiento en adyuvancia de CE y CUGE en CheckMate 577 se obtuvieron con independencia de localización, histología y expresión de PD-L11
SLE: supervivencia libre de enfermedad.
1. Kelly RJ, et al. Adjuvant Nivolumab in Resected Esophageal or Gastroesophageal Junction Cancer. N Engl J Med. 2021;384(13):1191-1203.



Hombre de 50 años*
MARIO
Tratamiento
- Revisión por el comité multidisciplinar:
- Se decide tratamiento pre-operatorio con QRT neoadyuvante (según esquema CROSS)
- Cirugía de esófago (esofagectomía de McKeown)
- AP: cáncer epidermoide de esófago. pT2N1M0
- Dehiscencia parcial de anastomosis cervical manejada con drenaje a través de herida
- Inicio con nivolumab adyuvante a las 12 semanas tras la cirugía, sin complicaciones relacionadas con el tratamiento.
QRT: quimirradioterapia; CROSS: neoadyuvancia con quimioterapia y radioterapia hiperfraccionada: Carboplatino: AUC 2 i.v. semanal (Días 1-8-15-22-29) Paclitaxel: 50mg/m2 i.v. semanal (Días 1-8-15-22-29) Radioterapia: 41.4 Gy en 23 fracciones de 1.8 G y cada una 5 días por semana; AP: anatomía patológica.
*Las imágenes no corresponden a pacientes reales


Caso 1

Cáncer de esófago
Evolución
- Completa 12 meses de tratamiento en adyuvancia.
- Revisión en consultas externas 3 años tras la cirugía sin signos de recidiva de enfermedad local ni a distancia.
*Las imágenes no corresponden a pacientes reales


CASO 2
TRATAMIENTO EN
PRIMERA LÍNEA



Caso 2

Adenocarcinoma Gástrico
Características demográficas y antecedentes personales
- Varón
- 39 años
- Sin antecedentes de interés
Enfermedad actual
- Paciente con dispepsia y pérdida ponderal de 8 kg en los últimos dos meses. Refiere astenia y anorexia, sin otras alteraciones
Diagnóstico
- EDA: con lesión ulcerada en antro gástrico
- AP: adenocarcinoma gástrico HER-2 negativo, MSI high, PD-L1 CPS=9
- Estudio de extensión con importante extensión adenopática regional y presencia de nódulos peritoneales supra e inframesocólicos sugestivos de malignidad
*Las imágenes no corresponden a pacientes reales
EDA: endoscopia digestiva alta; AP: anatomía patológica; HER2-: receptor del factor de crecimiento epidérmico humano negativo; MSI high: alta inestabilidad de los microsatélites; CPS: Puntaje positivo combinado.


Pregunta 1/4
Caso 2
¿Qué tratamiento propondrías para este paciente en base a sus características basales?1
A) Quimioterapia
B) Ramucirumab + quimioterapia
C) OPDIVO® + quimioterapia
D) Trastuzumab deruxtecán
En pacientes con inestabilidad de microsatellites, OPDIVO® + QT ha mostrado un beneficio significativo y clínicamente relevante sobre la supervivencia global1
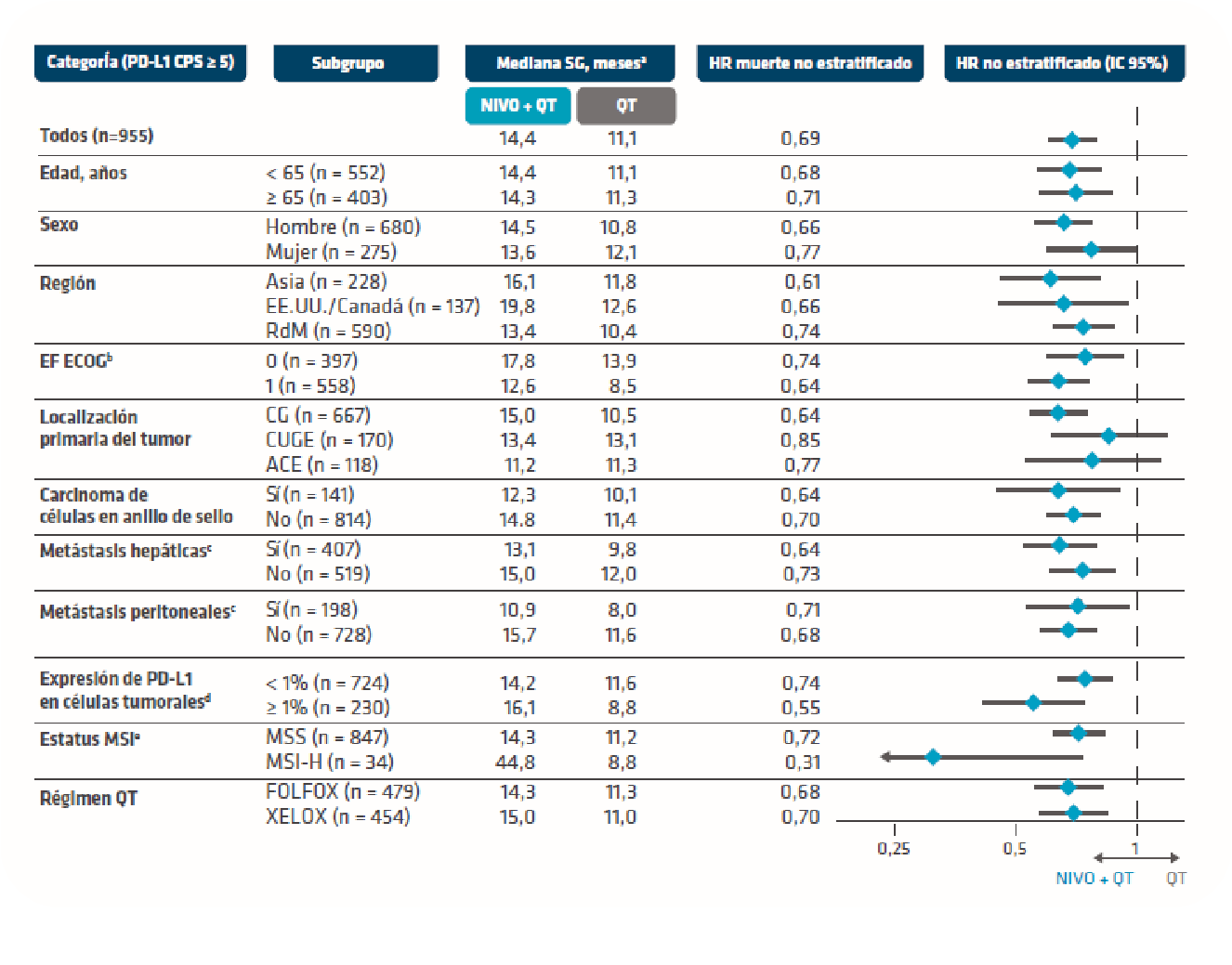
aSeguimiento mínimo: 48,1 meses; bEF ECOG 2, n = 4; cNo notificado, n = 29; dIndeterminado, no evaluable o no notificado, n = 1; eNo válido/no disponible, n = 74. PD-L1: Ligando de muerte programada 1; CPS: Puntuación positiva combinada; NIVO: Nivolumab; QT: Quimioterapia; EF: Estado funcional; ECOG: Grupo Oncológico Cooperativo del Este; RdM: Resto del mundo; CG: Cáncer gástrico; CUGE: Cáncer de la unión gastroesofágica; ACE: Adenocarcinoma de esófago; MSI: Inestabilidad de los microsatélites; MSS: Estabilidad de los microsatélites; MSI-H: Alta inestabilidad de los microsatélites; FOLFOX: Oxaliplatino + leucovorina + fluorouracilo; XELOX: Oxaliplatino + capecitabina; HR:Hazard ratio; IC: Intervalo de confianza.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31–June 4; Chicago, IL, & Online.


Pregunta 2/4
Caso 2
¿Cuáles son los resultados de supervivencia global de OPDIVO® + QT en primera línea de adenocarcinoma esofagogástrico obtenidos a los 3 y 4 años de seguimiento?
Une con flechas el tiempo de seguimiento con sus correspondientes tasas de supervivencia global.1
3 años
4 años
21%
19%
10%
17%
8%
OPDIVO® + QT duplicó la tasa de SG en comparación con QT a los 4 años de seguimiento1
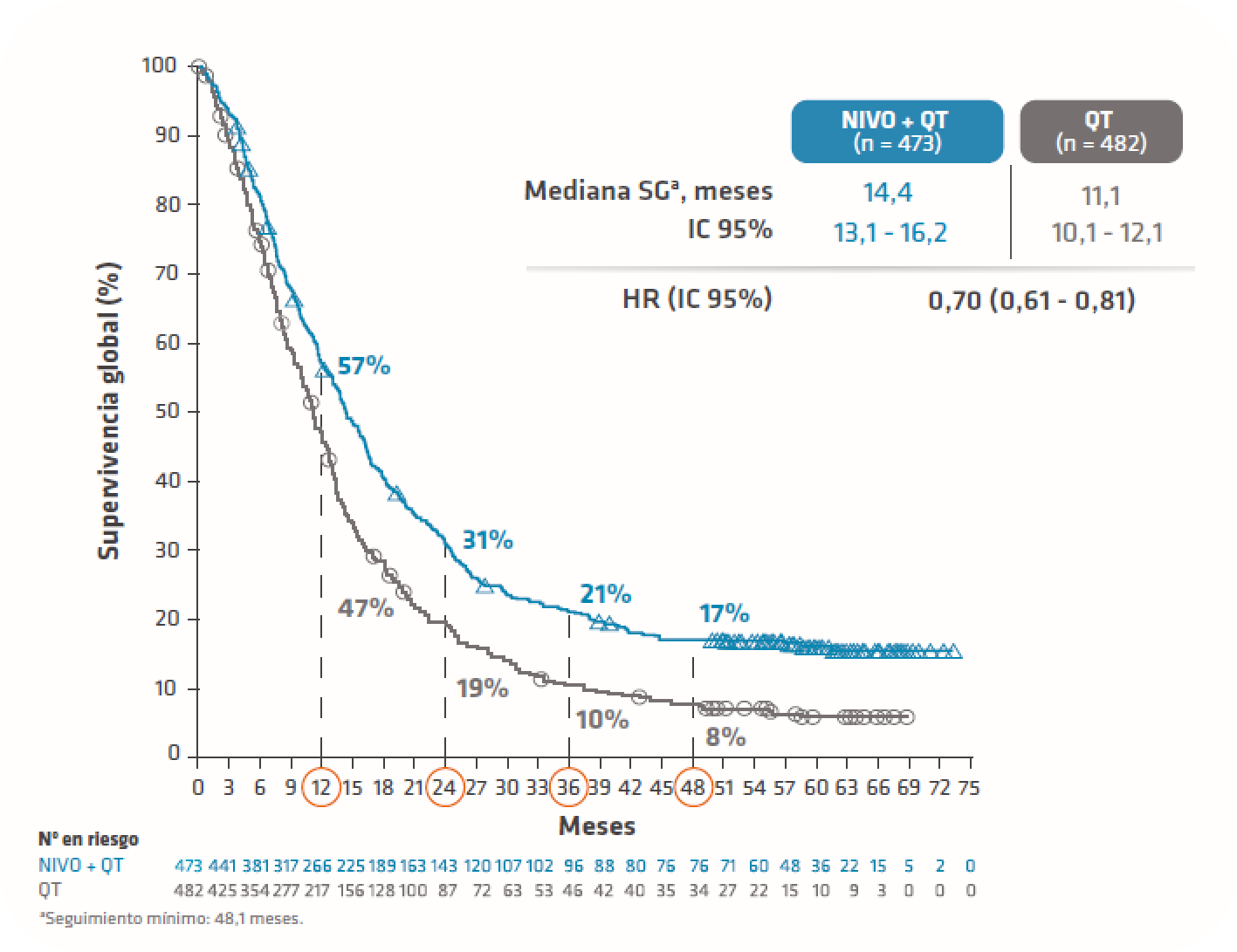
Traducida de Elimova E, et al. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31–June 4; Chicago, IL, & Online.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online


Pregunta 3/4
Caso 2
De entre las siguientes opciones, selecciona la que corresponde a la SLP alcanzada por OPDIVO® + QT en primera línea de adenocarcinoma esofagogástrico1
14,4 meses
8,3 meses
6,1 meses
SLP: supervivencia libre de progresión; QT: quimioterapia.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online.
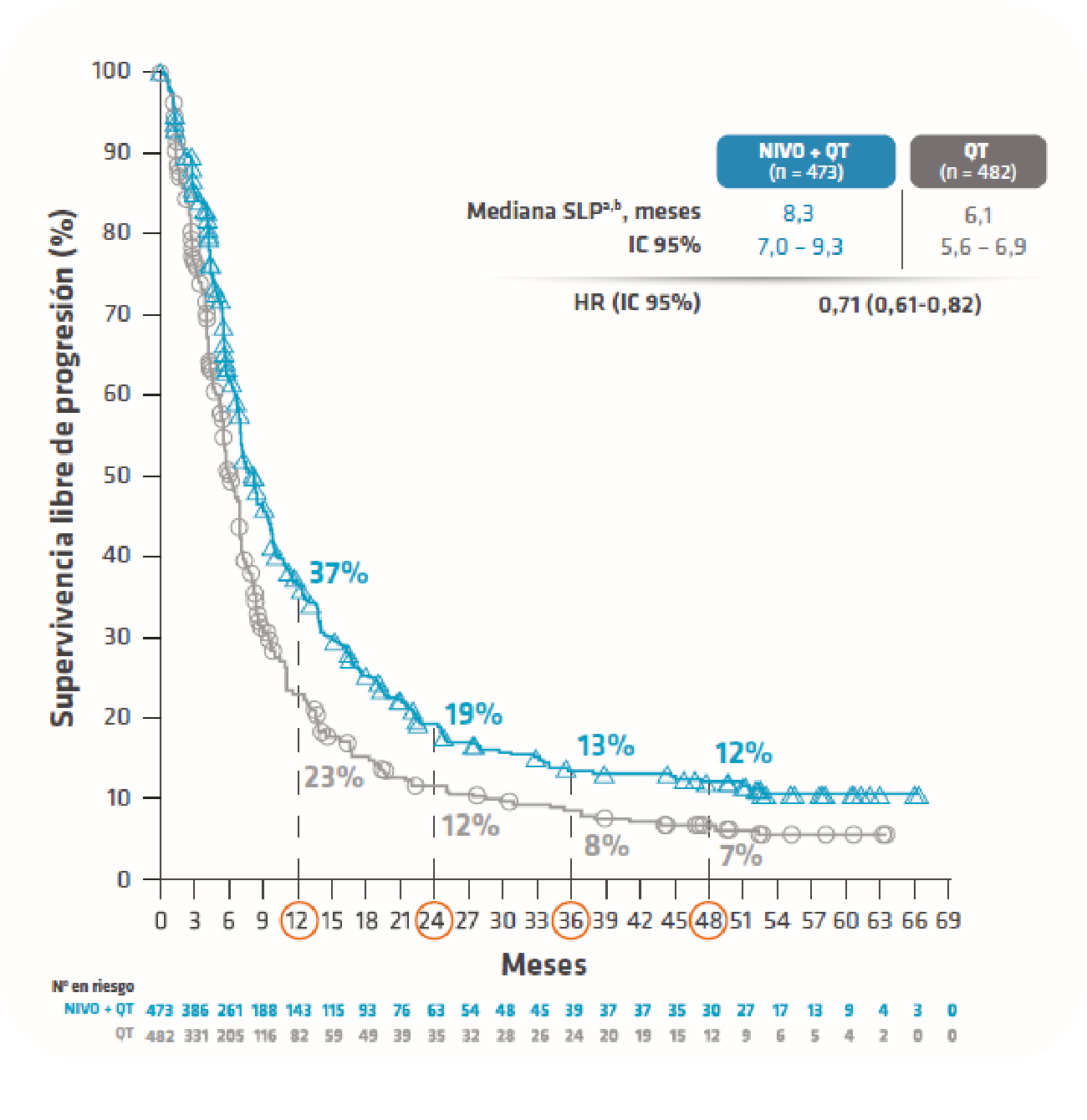
SLP: supervivencia libre de progresión; QT: quimioterapia.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online.


Pregunta 4/4
Caso 2
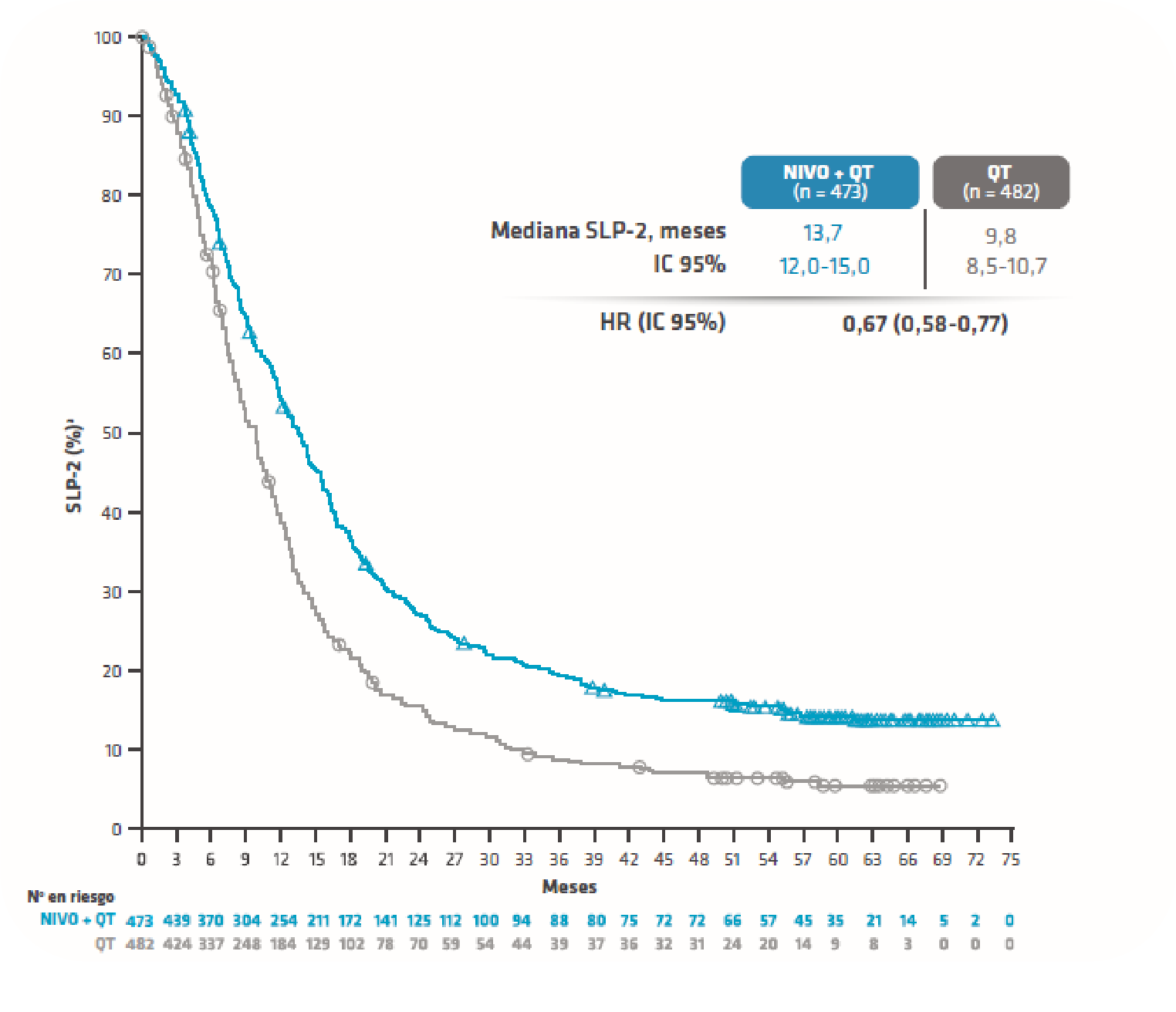
¿Sabe hasta qué punto impacta el tratamiento precoz con OPDIVO® + QT sobre la necesidad de una terapia subsecuente medida como SLP2?1
A) Aumento de 6 meses
B) Aumento de 9 meses
C) Aumento de 10 meses
D) Aumento de más de 12 meses
QT: quimioterapia; SLP2: supervivencia libre de progresión 2.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online.
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online.



Hombre de 39 años*
JORGE
Tratamiento y evolución
- Se inicia tratamiento con FOLFOX + OPDIVO®. Durante el tercer ciclo, el paciente experimenta reacción alérgica al oxaliplatino, motivo por el que se retira del esquema sin suspender el tratamiento con inmunoterapia
- El paciente presenta inicialmente una respuesta parcial importante, con desaparición de la totalidad de las lesiones a nivel peritoneal, así como disminución del tamaño de la lesión antral y de sus adenopatías locorregionales asociadas
- Tras 18 meses de tratamiento, el paciente continua con estabilidad de enfermedad y con adecuada tolerancia oral a sólidos y a líquidos
FOLFOX: Oxaliplatino + leucovorina + fluorouracilo.
*Las imágenes no corresponden a pacientes reales


CASO 3
TRATAMIENTO EN
PRIMERA LÍNEA



Caso 3

Adenocarcinoma de la unión Gastroesofágica
Características demográficas y antecedentes personales
- Varón
- 72 años
- HTA (hipertensión arterial) en tratamiento
- DM2 (Diabetes Mellitus tipo 2) en tratamiento con metformina
Enfermedad actual
- Debuta con pérdida de 10 kg de peso y disfagia a sólidos y líquidos, asociados a astenia de moderados esfuerzos
Diagnóstico
- EDA (endoscopia digestiva alta): lesión infranqueable endoscópicamente a nivel de UEG-antro gástrico
- AP (anatomía patológica): adenocarcinoma de la unión gastroesofágica, PD-L1 CPS=12, MSS (estabilidad de microsatélites), HER-2 (receptor 2 del factor de crecimiento epidérmico humano) negativo
- TC (tomografía computerizada): tumor a nivel de la unión gastroesofágica con lesión hepática en segmento IV sugestiva de malignidad


Pregunta 1/4
Caso 3
El tratamiento con OPDIVO® + QT en primera línea del adenocarcinoma esofagogástrico ha sido capaz de establecer el concepto de largos supervivientes con esta patología, lo que ha supuesto un cambio en el paradigma de esta enfermedad.
¿Sabrías precisar en qué medida aumenta la tasa de SG con la combinación OPDIVO® + QT comparada con QT a los 4 años?1
No aumenta
X1,5 veces
X2 veces
OPDIVO® + QT duplicó la tasa de SG a 4 en comparación con la QT sola1
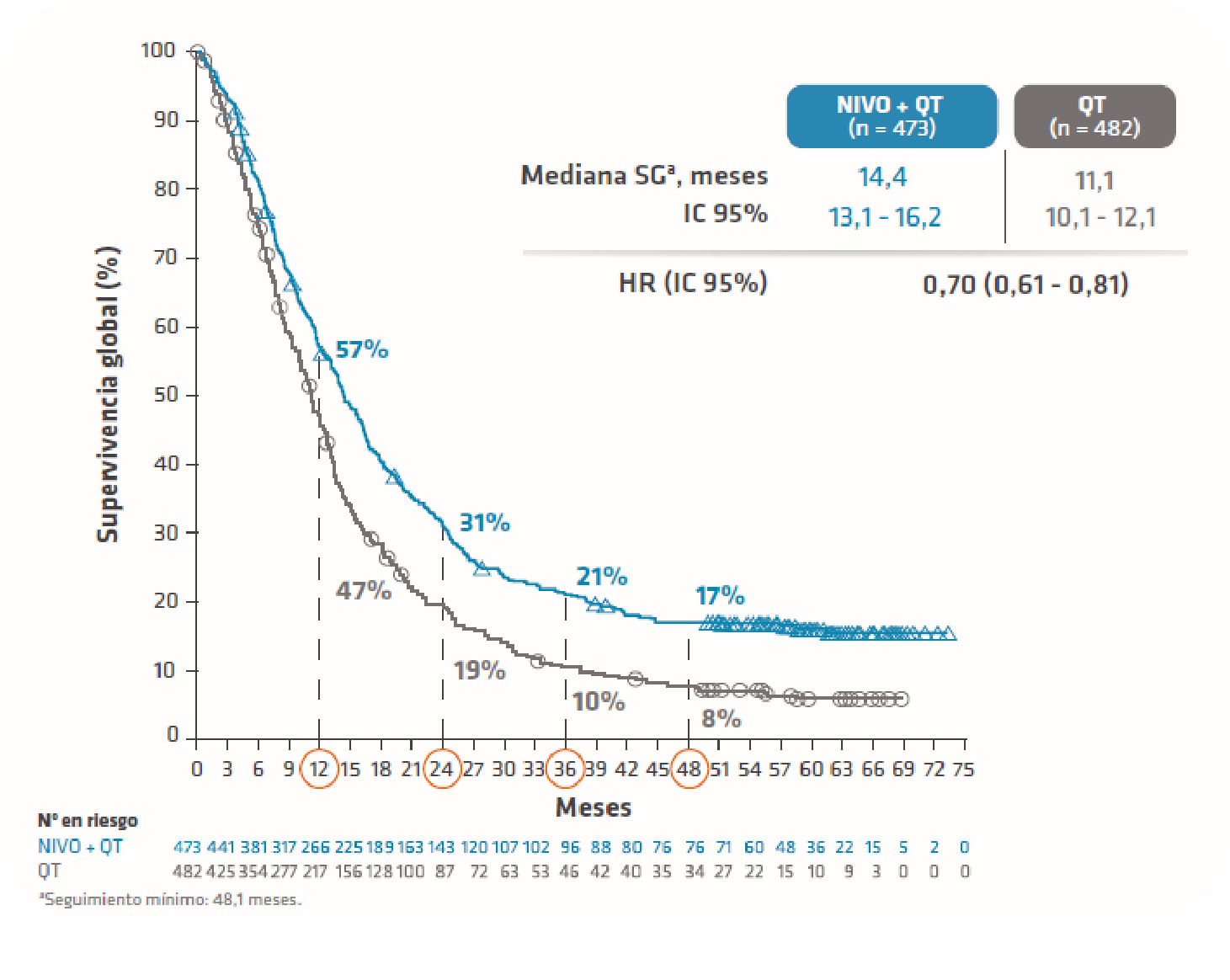
1. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study. [Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31-June 4; Chicago, IL, & Online.


Pregunta 2/4
Caso 3
Indique con verdadero o falso las siguientes afirmaciones sobre el perfil de seguridad de OPDIVO® + QT en primera línea adenocarcinoma esofagogástrico1
Se produjeron acontecimientos AART de grado 3/4 en < 5% de los pacientes con OPDIVO® + QT con un seguimiento superior a 3 años prolongado en las distintas categorías
Se observaron nuevas señales de seguridad con OPDIVO® + QT después de 4 años de seguimiento
Los AART de grado 3/4 más frecuentes para OPDIVO® + QT fueron la neutropenia, disminución del recuento de neutrófilos, anemia y aumento de la lipasa.
AART: Acontecimiento adverso relacionado con el tratamiento; QT: Quimioterapia.
1. Janjigian YY, et al. First-Line Nivolumab Plus Chemotherapy for Advanced Gastric, Gastroesophageal Junction, and Esophageal Adenocarcinoma: 3-Year Follow-Up of the Phase III CheckMate 649 Trial. J Clin Oncol. 2024;42(17):2012-2020. 2. Elimova E, et al. Nivolumab plus chemotherapy vs chemotherapy as first-line treatment for advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: 4-year follow-up of the CheckMate 649 study.[Poster 4040]. Presented at the 2024 American Society of Clinical Oncology (ASCO) Annual Meeting; May 31–June 4; Chicago, IL, & Online.
Lorem ipsum dolor sit amet consectetur adipisicing elit. Itaque aut maxime, corrupti recusandae error debitis eos ratione. Excepturi aspernatur perferendis eos autem, alias ab porro, a perspiciatis, necessitatibus corrupti cum.
* Lorem ipsum dolor sit amet consectetur, adipisicing elit.


Pregunta 3/4
Caso 3
¿Podría indicar la pauta posológica de nivolumab para sus pacientes con adenocarcinoma de la unión gastroesofágica?1
Cada 2 semanas
Cada 3 semanas
Cada 2 o 3 semanas
1. Ficha técnica de OPDIVO® (Nivolumab).
OPDIVO® proporciona una pauta posológica flexible para sus pacientes con adenocarcinoma de la unión gastroesofágica1
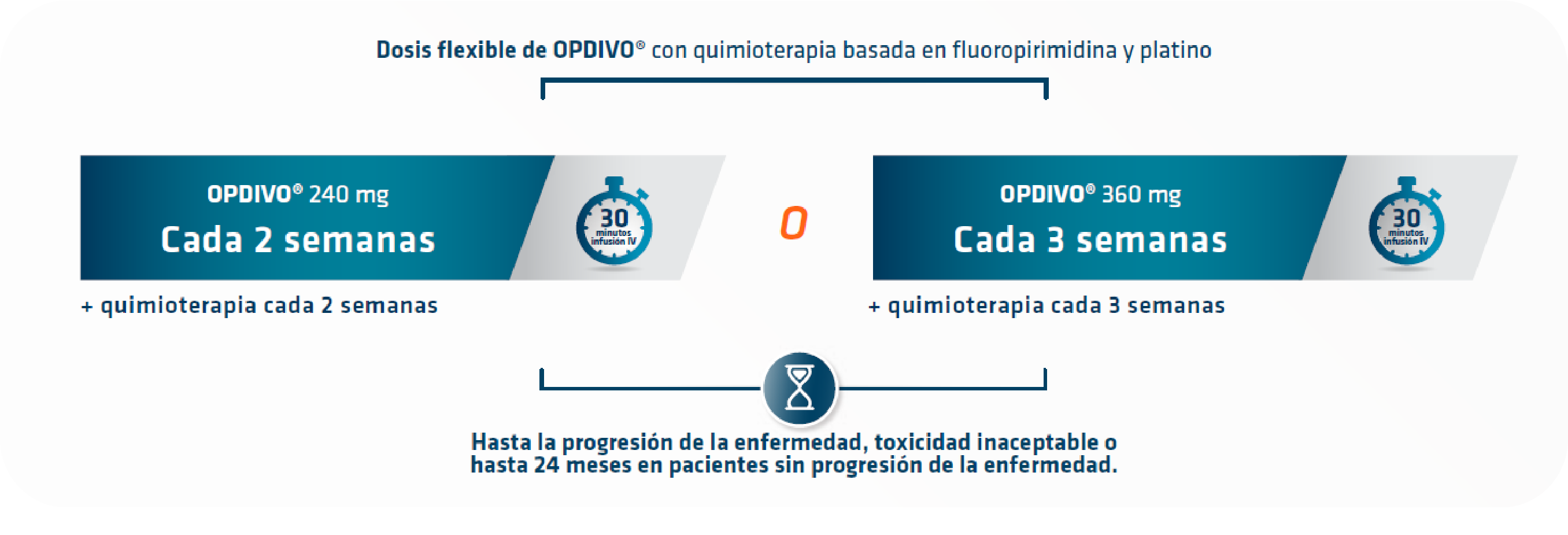
1. Ficha técnica de OPDIVO® (Nivolumab).


Pregunta 4/4
Caso 3
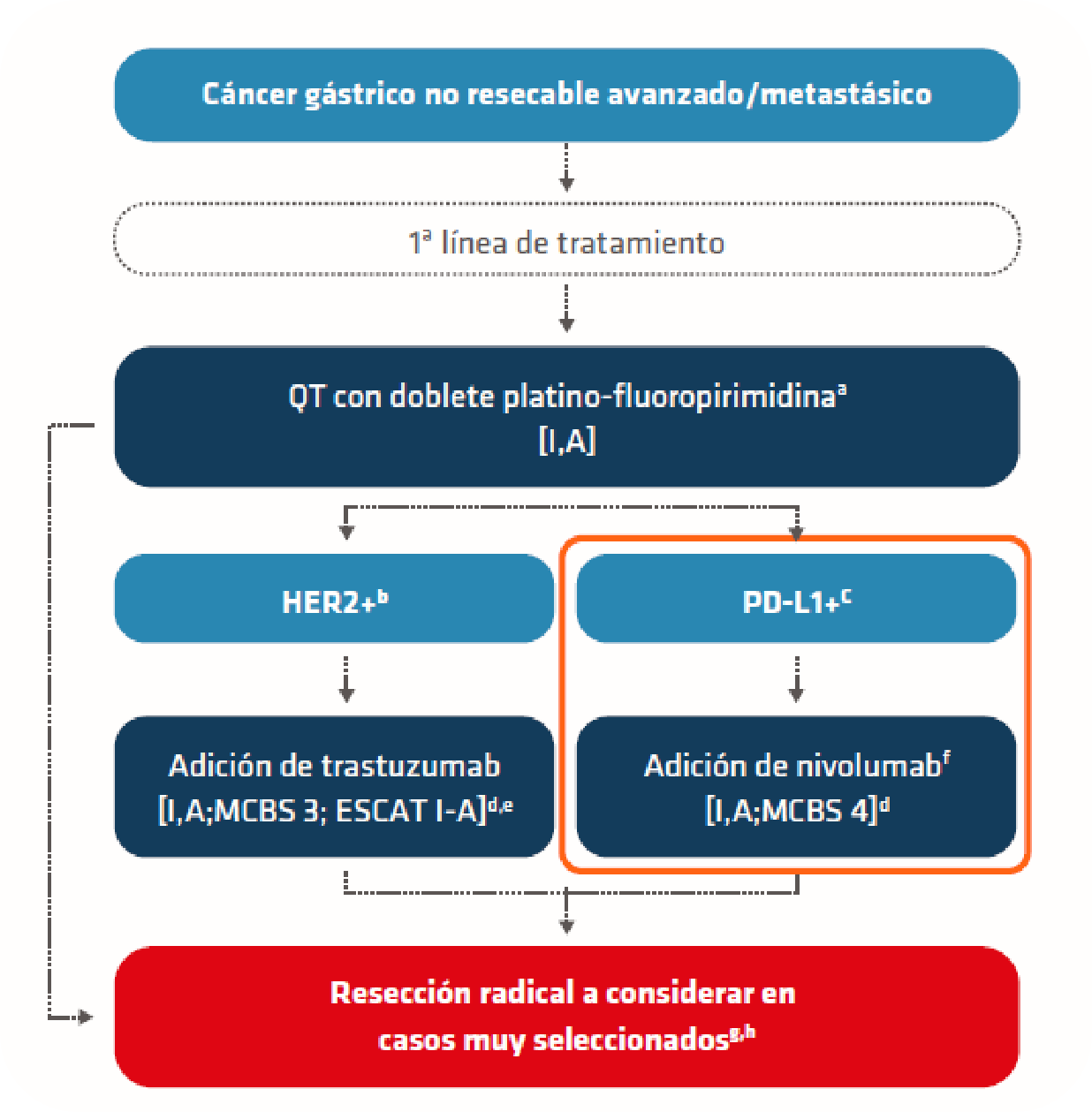
Ordena las siguientes piezas para componer el algoritmo de tratamiento de ESMO para para el tratamiento en 1L del cáncer gástrico irresecable avanzado metastásico1
Resección radical a considerar en casos muy seleccionadosg,h
PD-L1+b
Adición de trastuzumab [I,A;MCBS 3; ESCAT I-A]d,e
1ª línea de tatamiento
Cáncer gástrico no resecable avazado/metastásico
Adición de nivolumabf [I,A;MCBS 4]d
HER2+b
QT con doblete platino-fluoropirimidinaa [I,A]
PD-L1: ligando 1 de muerte programada; HER2-: receptor del factor de crecimiento epidérmico humano negativo; MCBS: Escala de Magnitud de Beneficio Clínico (por sus siglas en inglés, Magnitude of Clinical Benefit Scale);ESCAT: Escala ESMO de accionabilidad clínica de dianas moleculares (por sus siglas en inglés, ESMO Scale for Clinical Actionability of molecular Targets); QT: quimioterapia.
aLos compuestos de platino recomendados son oxaliplatino o cisplatino. Se prefiere el oxaliplatino, especialmente en pacientes de edad avanzada. Las fluoropirimidinas recomendadas son 5-FU intravenoso, capecitabina oral o S-1 oral. Irinotecan-5-FU puede considerarse una opción alternativa para los pacientes que no toleran los compuestos de platino.
bHER2 IHQ 3+ o IHQ 2+/FISH-positivo.
c estado de PD-L1 debe notificarse según CPS.
dSe utilizó ESMO-MCBS v1.1 para calcular las puntuaciones de las terapias/indicaciones aprobadas por la EMA o la FDA. Las puntuaciones han sido calculadas por el Grupo de Trabajo ESMO-MCBS y validadas por el Comité de Guías de la ESMO (https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-evaluation-forms).
eLas puntuaciones ESCAT se aplican únicamente a las alteraciones genómicas. Estas puntuaciones han sido definidas por los autores de las directrices y validadas por el Grupo de Trabajo de Investigación Traslacional y Medicina de Precisión de la ESMO.
fNivolumab + QT se recomienda para el cáncer gástrico avanzado no tratado con un PD-L1 CPS 5 (aprobado por la FDA sin restricción de PD-L1 CPS, aprobado por la EMA para PD-L1 CPS 5).
gNo se recomienda la gastrectomía en el cáncer gástrico metastásico a menos que sea necesaria para paliar los síntomas.
hEn general, la resección de metástasis no puede recomendarse, pero podría considerarse como un abordaje individual en casos muy seleccionados con enfermedad oligometastásica y respuesta a QT.
1. Lordick F, et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022;33(10):1005-1020.



Hombre de 72 años*
ANTONIO
Características demográficas y antecedentes personales
- Varón
- 72 años
- HTA (hipertensión arterial) en tratamiento
- DM2 (Diabetes Mellitus tipo 2) en tratamiento con metformina
Enfermedad actual
- Debuta con pérdida de 10 kg de peso y disfagia a sólidos y líquidos, asociados a astenia de moderados esfuerzos
Diagnóstico
- EDA (endoscopia digestiva alta): lesión infranqueable endoscópicamente a nivel de UEG-antro gástrico
- AP (anatomía patológica): adenocarcinoma de la unión gastroesofágica, PD-L1 CPS=12, MSS (estabilidad de microsatélites), HER-2 (receptor 2 del factor de crecimiento epidérmico humano) negativo
- TC (tomografía computerizada): tumor a nivel de la unión gastroesofágica con lesión hepática en segmento IV sugestiva de malignidad
Tratamiento y evolución
- Se inicia tratamiento con FOLFOX + nivolumab
- No desarrolla ningún acontecimiento adverso inmunorrelacionado y presenta una respuesta patológica completa que mantiene todavía a día de hoy y que le lleva a mantener el tratamiento con nivolumab (48 meses desde inicio del mismo) por decisión propia de su médico, en base a la respuesta al tratamiento y extendiendo la recomendación de la ficha técnica. Mantiene buena calidad de vida.
- Se retiró el oxaliplatino y continua a día de hoy con el esquema de 5FU y nivolumab
FOLFOX: leucovorina cálcica (ácido folínico), fluorouracilo y oxaliplatino; HTA: hipertensión arterial; DM2: diabetes mellitus tipo 2; EDA: endoscopia digestiva alta; AP: anatomía patológica; MSS: estabilidad de microsatélites; HER2-: receptor 2 del factor de crecimiento epidérmico humano negativo; TC: tomografía computerizada; 5-FU: 5 fluorouracilo.
*Las imágenes no corresponden a pacientes reales


GRACIAS
POR PARTICIPAR




-
-

-
-

-
-
